|
HPV16型早期蛋白基因后端粒酶的活性表達
第一軍醫大學學報1999年第19卷第5期
人成纖維細胞轉染
吳 翔 朱 冰 楊光彩 徐 鈐
摘 要 用已構建的含有HPV16的早期蛋白的質粒載體:pME6SN、pME7SN和pME6E7SN經脂質體介導,轉入正常的人成纖維細胞。經G418選擇篩選及鑒定后證實,E6、E7、E6E7轉化的細胞壽命延長;E6、E6E7表達的細胞中有端粒酶的表達,E7表達的細胞中未能檢測到端粒酶的表達。提示端粒酶的表達是細胞轉化后的一個后續事件。
關鍵詞:人乳頭瘤病毒 E6 E7 人成纖維細胞 端粒酶
自70年代末以來,不斷增加的流行病學、病理學和分子生物學的證據表明:人乳頭瘤病毒(Human papillomavirus, HPV)與宮頸癌的關系非常密切。宮頸癌及其癌株細胞(Hela)中可檢測到特異性的HPV早期蛋白,而其中有些蛋白(如HPV16E6、E7蛋白)的編碼基因被證實為轉化基因。1996年,Klingelhutz[1]等用人乳頭瘤病毒的E6、E7、E6E7基因轉入正常人角質細胞和上皮細胞后發現,細胞出現生存代數延長和永生化現象,證實當時細胞永生化與端粒酶的表達有關。1997年,Shiga[2]將HPV16的E6、E7、E6E7基因轉入人成纖維細胞后,發現細胞出現形態學方面的改變,細胞中出現端粒酶的表達。
本研究率先在國內用檢測端粒酶活性表達的方法進一步研究癌基因在腫瘤發生、發展中的作用。通過研究人成纖維細胞轉染HPV16E6、E7癌基因對端粒酶的活性表達作用,進一步研究HPV16E6、E7基因的致癌機理及其相互關系,從而為人乳頭瘤病毒的早期診斷和治療探討新的手段和途徑。
1 實驗材料
1.1材料
1.1.1 質粒 pMSN重組質粒由pMDSG質粒改造構建而成。在pMSN的Xba1位點分別插入HPV16E6、E7和E6E7基因,所得重組質粒分別稱為pME6SN,pME7SN和pME6E7SN,由德國de Villiers博士惠贈,本室保存。
1.1.2引物 CX、TS、P1、P2、P3、P4、P5、P6,由中科院上海植物生理所植物分子遺傳國家重點實驗室合成(表1)。
表1 實驗中使用的引物
Tab. 1 Primers in assay
|
Name
|
Sequence
|
Usage
|
|
CX
|
5’CCCTTACCCTTACCCTTACCCTAA3’ |
Amply telomerase |
|
TS
|
5’AATCCGTCGAGCAGAGTT3’ |
Amply telomerase |
|
P1
|
5’TTAGAACAGCAATACAACAAAC |
Amply E6 fragment |
|
P2
|
5’ACCGGTCCACCGACCCCTTA |
Amply E6 fragment |
|
P3
|
5’TAGAGTCACACTTGCAACAA |
Amply E7 fragment |
|
P4
|
5’GAGACAACTGATCTCTACTG |
Amply E7 fragment |
|
P5
|
5’TTAGAACAGCAATACAACAAAC |
Amply E6E7 fragment |
|
P6
|
5’TAGAGTCACACTTGCAACAA |
Amply E6E7 fragment |
1.1.3 研究對象 人成纖維細胞(Normal human fibroblast, NHF)
1.2 主要試劑
1.2.1 細胞培養試劑 DMEM高糖培養基(Gibco BRL公司),胎牛血清(杭州四季青公司),LIPOFECTAMINE( Gibco BRL公司),G418( Gibco BRL公司)。
1.2.2 提細胞DNA裂解液 廣州達安醫學診斷公司。
1.2.3 TRAP法中使用的細胞裂解工作液I (4℃保存) 10 mol/L Hepes-KOH,1.5 mol/L MgCl2,10 mol/L KCl,1 mol/L DTT。
1.2.4 TRAP法中使用的細胞裂解工作液II(4℃保存) 10 mol/L Tris-HCl (pH7.5),1 mol/L MgCl2,1 mol/L EGTA,0.1 mol/L AEBSF,0.55%CHAPS,5 mol/L b -巰基乙醇,10%甘油。
1.2.5 酶轉錄反應緩沖液成分 20 mol/L Tris-Cl(pH8.3),1.5 mol/L MgCl2,63 mol/L KCl,0.005% Tween-20, 1 mol/L EGTA,50 μmol/L dNTP,1μg T4g32蛋白。
2 實驗方法
2.1細胞培養及收獲
2.1.1 人成纖維細胞的傳代培養 取傳代培養的人成纖維細胞,棄去瓶中的培養液,加入0.25%的胰蛋白酶消化。按1:3的比例傳代。置37℃,5%CO2,飽和濕度環境下培養,建立皮膚組織成纖維細胞的傳代體系。
2.1.2 培養細胞的收獲 若需收集細胞,將消化后的細胞全部轉入離心管中,8 000 g%26acute; 10 min,室溫離心,收集細胞團塊。
2.2 HPV16的早期蛋白基因轉染人成纖維細胞 參見文獻[3]及GIBCO公司Lipofectamin試劑產品說明書上的方法進行,傳第3代(1~2)%26acute; 105個細胞到60 mm的培養皿內。約2周后,可見有抗性克隆形成,待其逐漸長大,出現轉化灶后,采用刮除法以獲得純的轉化細胞群。
2.3 轉染細胞的鑒定 取滅菌的0.5 ml離心管一個,PCR反應總體積為50μl,收獲培養的細胞加入提細胞DNA裂解液,100℃水浴處理10 min,1 000 g×10 min離心后取上清作為反應模板。加50 pmol/L的引物P5-P10(引物配對方式見實驗材料1.1.2部分,分別擴增E6,E7,E6E7片段)各2μl,模板0.5μg等反應液,混勻后,進行PCR擴增。取5μl反應液,在8%的聚丙烯酰胺凝膠上穩壓150 V電泳2 h,銀染。
2.4 細胞轉化后端粒酶活性的測定
2.4.1 細胞中端粒酶的提取,表達水平的測定 參照文獻[4]的TRAP方法
2.4.2 非放射性銀染技術對TRAP產物進行觀察
2.4.2.1電泳 取TRAP產物30 m l及標準分子量(PBR322DNA/HaeIII)1 m g,分別與適量加樣緩沖液混合上樣進行12%的聚丙烯酰胺凝膠電泳,電壓200 V,恒壓電泳4 h。
2.4.2.2銀染 取下凝膠,置10%乙醇內固定10 min,水洗2次;1%硝酸內脫色3 min,水洗2次;0.012 mol/L硝酸銀染色液避光染色20 min,水洗3次;0.28 mol/L Na2CO3-0.019%甲醛顯影液,直至產物信號足夠強而背景不致過高為止;用10%的冰醋酸終止反應,水漂洗后制干膠保存或拍照。
2.4.2.2 對圖象進行計算機掃描分析 將染好的膠置于凝膠圖象分析系統拍照。
3 實驗結果
3.1 轉化細胞的克隆及篩選 正常人成纖維細胞(圖1-A)伸展良好,折光性較弱,單層生長,有方向性和接觸抑制作用。在含G418 (400 mg/L)的培養液中,第3 天開始死亡(圖1-B),而由質粒r MSN重組系列轉染的人成纖維細胞經G418(400 mg/L)篩選培養2周后,逐漸形成大小不等的細胞轉化灶(圖2)。
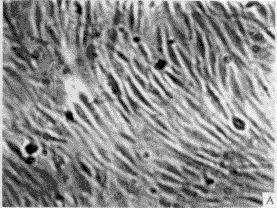
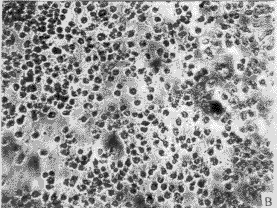
圖1 正常傳代培養的人成纖維細胞(A)及加入G418后的正常人成維細胞(B)
Fig. 1 Normal NHF (A) and normal NHF added with G418(B)
a: Primary cells at passage (P) 3,characterized by stretching well, growth with direction and contact-inhibition; B: Primary cells were introduced by blank vectors, All of them died after 5 days with G418 400 mg/L ×100
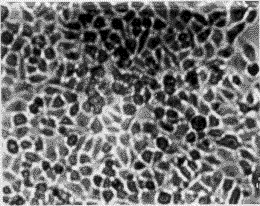
圖2 pME6SN、pME7SN、pME6E7SN轉染的人成纖維細胞2周后出現轉化灶
Fig. 2 NHFs introduced by pME6SN, pME7SN, pME6E7SN
producing transfected clone after 2 weeks ×100
經pME6SN、pME7SN、pME6E7SN轉化的細胞出現細胞大小不一,生長方向紊亂,接觸抑制消失,呈重疊性生長,伸展性較差,折光性強,形態類似于上皮細胞等惡性細胞表型特征。而不含HPV任何基因的空載體r MSN轉化的細胞,具有接觸抑制作用,有方向性單層、不重疊生長,其細胞特征與正常人成纖維細胞生長相似。
3.2轉化細胞的鑒定結果 所設計的3對引物分別對HPV的E6、E7、E6E7基因是特異的,擴增后的片段為140、138和387 bp,與預期的結果完全一致(圖3)。
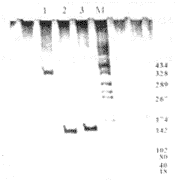
圖3 轉化細胞的鑒定
Fig. 3 Identification of cells transformed by PCR, 8% non-denaturing PAGE ,150 V for 2 hours and silver-staining
1: NHF introduced by pME6E7SN; 2: NHF introduced by pME7SN; 3: NHF introduced by pME6SN; M: marker
3.3 人成纖維細胞經HPV16早期蛋白基因轉染后檢測端粒酶活性 從不同細胞端粒酶表達的時間先后來看,HPV16E6基因轉染人成纖維細胞后的第15代(從細胞原代培養開始計算生存代數,下同)出現端粒酶的表達;HPV16E7基因轉染人成纖維細胞后直至細胞死亡(第19代),一直未檢測到端粒酶的表達;HPV16E6E7基因轉染人成纖維細胞后的第14代即可檢測到端粒酶的表達;而正常細胞和經pMSN轉染的細胞只能生長至第10代和第13代,未檢測到端粒酶的表達(圖4)。
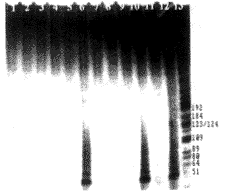
圖4 pMSN重組質粒轉染人成纖維細胞后端粒酶的表達情況
Fig.4 Telomerase activities of NHFs transfected by pMSN recombinant plasmids were analyzed by TRAP method
1: NHF; 3: NHF introduced by pMSN; 5: NHF introduced by pME6SN; 7: NHF introduced by pME7SN; 9: NHF introduced by pME6E7SN; 11: Hela cell; 2,4,6,8,10,12: cell extracts pretreated at 100℃ for 10 min; 13: marker (pBR322DNA/HaeIII)
4 討論
細胞經pMSN、pME6SN、pME7SN、pME6E7SN質粒載體轉染后,僅在pME6SN、pME6E7SN 轉染的細胞檢測出端粒酶的表達,而在pMSN、pME7SN轉染的細胞中未能檢測出端粒酶的表達。HPV16E6E7基因轉染的細胞中端粒酶出現最早,在轉染后,細胞生長的第14代即有檢出信號,HPV16E6基因轉染的細胞要到細胞生長的第15代才有檢出信號。這與Klingelhutz[5]的實驗結果吻合,Klingelhutz認為細胞轉入HPV16基因后早期就有端粒酶的表達。
實驗中還發現E6,E6E7基因可致使細胞表達端粒酶,E7基因不能激活端粒酶的表達,但細胞依然出現了惡性轉變特性。這與Stoppler[6]的實驗結果相同。
由HPV16E7轉染的細胞,在每代生長時,都檢測了端粒酶的活性,但一直未發現端粒酶出現活性,在細胞正常傳代的第19代出現細胞衰老現象,無法繼續傳代而死亡。正常細胞及經空質粒載體轉染的細胞傳代至第10代和第13代死亡。
這些時間數據同時也說明,人成纖維細胞經E6、E7、E6E7轉染后確實能延長細胞的壽命,細胞壽命的延長與端粒酶的表達可能有關,同時也說明腫瘤發生是多因素引起的。
在我們研究的轉化細胞中E6,E6E7基因轉染的細胞中可以檢出端粒酶,空質粒載體及E7基因轉染的細胞中不能檢測到端粒酶。E7基因轉染后的細胞,雖然我們觀察到細胞形態學出現變化,但端粒酶活性的檢測結果始終是陰性,或許E7基因維持細胞的惡性表型,并不完全依靠端粒酶的表達,可能還有其他機制來維持端粒的長度,如重組途徑,反轉錄途徑或救援途徑[7]。在酵母的研究中已得到證實[8]。在Kim[4]等人的研究中也發現雖然多數腫瘤組織中端粒酶活性很高,但仍有少數惡性腫瘤不能觀察到該酶的活性,推測有可能是這些細胞逃逸了M1期,具有一定的增殖能力,但端粒酶尚未被激活,所以并不能無限增殖。
可能HPV16E6基因像降解p53一樣,使另一抑癌基因降解而導致端粒酶基因被激活,而不受抑制地表達,在這一點上E7可能不同,它不能使另一抑癌基因被降解,從而無法對端粒酶的表達出現影響,不顯示出端粒酶的激活表達,這一推測有待于在今后的研究工作中進一步證實。
作者簡介:吳 翔,男,1970年出生;發表論文兩篇;電話81936697
作者單位:吳 翔 楊光彩 徐 鈐 第一軍醫大學生物化學教研室,廣州,510515 朱 冰 兒童醫院病毒室,廣州,510130
參考文獻
1 Klingelhutz AT, Foster SA, McDougall JK et al. Telomerase activation by the E6 gene product of human papillomavirus type16. Nature 1996,380(6569):79
2 Shiga T, Shirasawa H, Shimiyu K. Normal human fibroblasts immortalized by introduction of human papillomavirus type 16(HPV16) E6-E7 genes. Microbiol Immunol,1997,41(4):313
3姜 泊. 分子生物學常用實驗方法,第二版.北京:人民軍醫出版社.1996, 34~41
4 Kim NW, Piatyszek MA, Prowse KR. Specific association of human telomerase activity with immortal cells and cancer. Science, 1994, 266(23):2011
5 Klingelhutz AJ, Foster SA, McDougall JK. Telomerase activation by the E6gene product of human papillomavirus type16. Nature, 1996, 380 (6569):79
6 Stoppler H,Hartmann DP,Sherman J. The human papillomavirus type16E6 and E7 oncoproteins dissociate cellular telomerase activity from the maintenance of telomere length. J Biol Chem, 1997,272(20):13332
7 Pluta AF, Zakian VA. Recombination occurs during telomere formation in yeast. Nature, 1989,337(6206):429
8 Mceachern MJ, Cohn M, Blackburn EH. The yeast kluyveromyces lactis as a model system to study telomere length regulation and the ability of cells to grow in the absence of telomerase. PAACR, 1995,36:670
|